Parkinson
-
De ziekte van Parkinson is een chronisch progressieve neurodegeneratieve aandoening waarbij bradykinesie (trager bewegen) op de voorgrond staat. Het is de op twee na meest voorkomende aandoening binnen de chronisch progressieve neurodegeneratieve ziektebeelden; de ziekte van Alzheimer staat daarbij op nummer één. De ziekte van Parkinson start gemiddeld rond het 60ste levensjaar [1].
-
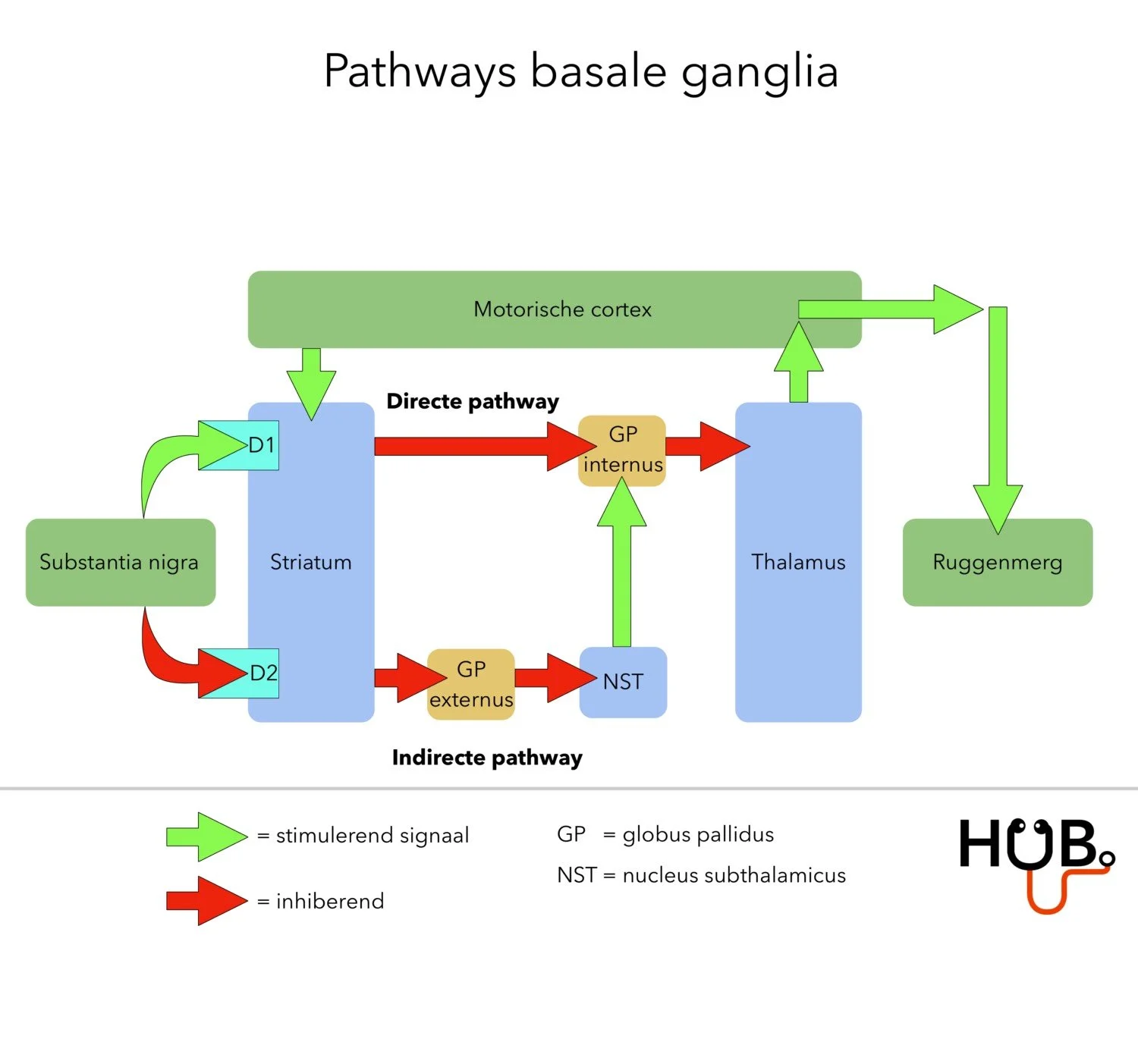
De substantia nigra (AFBEELDING 1) is opgebouwd uit twee onderdelen: de pars compacta en pars reticulata. Bij de ziekte van Parkinson speelt het verlies van dopamine producerende neuronen in de substantia nigra pars compacta een belangrijke rol. De substantia nigra maakt onderdeel uit van de basale ganglia. De basale ganglia zijn betrokken bij het reguleren van bewegingen door invloed uit te oefenen op de thalamus, van waaruit signalen naar de motorische cortex gaan om een gecontroleerde beweging uit te kunnen voeren (AFBEELDING 2). De gedachte is dat door verlies van neuronen in de substantia nigra pars compacta er minder dopamine wordt afgegeven in het striatum (AFBEELDING 1). Het gevolg is een verstoorde balans tussen de directe en indirecte banen (AFBEELDING 2) van de basale ganglia waardoor de thalamus sterker wordt geremd, wat uiteindelijk leidt tot remming van bewegingen en de karakteristieke tremor [2].
Niet alleen de dopaminerge neuronen in de substantia nigra zijn aangedaan bij de ziekte van Parkinson. In veel verschillende soorten neuronen zijn ophopingen van eiwitten te vinden. Daarbij ontstaan insluitlichaampjes, de zogenaamde Lewy bodies. Dit zijn ophopingen van alfa-synucleïne eiwitten. De eerste ophopingen van eiwitten treden op in de medulla oblongata (AFBEELDING 3) en gebieden van de hersenen betrokken bij reuk. Dit gebeurt tijdens de niet-motorische, prodromale fase van de ziekte. Naarmate het ziekteproces vordert, verspreiden deze zich steeds meer door de hersenen. Wanneer de substantia nigra wordt aangetast, ontstaan de kenmerkende motorische symptomen. Ook neuronen die andere neurotransmitters gebruiken zoals acetylcholine, noradrenaline en serotonine raken beschadigd. Uiteindelijk worden zelfs grote delen van de hersenschors aangetast. De wijde verspreiding van het ziekteproces verklaart waarom de ziekte van Parkinson gepaard gaat met een groot aantal niet-motorische symptomen die niet worden veroorzaakt door een dopaminetekort, zoals obstipatie en anosmie (geen vermogen tot ruiken) [1].
De precieze oorzaak van de ophoping van eiwitten en het verlies van dopaminerge neuronen is onbekend, maar zowel een genetische aanleg als omgevingsfactoren (zoals in aanraking komen met pesticiden) lijken een rol te spelen.
-
Bradykinesie (trager bewegen) is het meest voorkomende motorische symptoom bij de ziekte van Parkinson.
Rigiditeit (stijfheid).
Rusttremor (trilling).
Houdings- en balansstoornissen. Dit treedt meestal pas op in een later stadium van de ziekte.
Bovenstaande combinatie van motorische symptomen wordt aangeduid met de term parkinsonisme. In het beginstadium van de ziekte zijn er vaak alleen nog motorische symptomen aan één kant van het lichaam. Later breidt dit zich uit naar beide kanten. De lichamelijke problemen nemen over de jaren geleidelijk toe. Het lopen gaat steeds moeizamer en patiënten gaan schuifelend en voorovergebogen lopen. Ook kan ‘freezing’ optreden; hierbij blijft de patiënt, wanneer deze eigenlijk zou willen gaan lopen, als het ware vastgeplakt aan de grond [3].
Niet-motorische symptomen die vaak voorkomen bij de ziekte van Parkinson zijn cognitieve stoornissen, die zich regelmatig verder ontwikkelen tot een dementie, en psychiatrische stoornissen zoals depressie, angst, impulscontrolestoornissen (bijvoorbeeld excessief gokken of hyperseksualiteit) en psychose. Psychoses worden veroorzaakt door de ziekte, maar kunnen worden uitgelokt door de medicatie of een infectie. Tot slot kan medicatie een rol spelen bij het optreden van impulscontrolestoornissen [4].
-
Omdat de ziekte van Parkinson progressief verloopt, neemt de mobiliteit steeds verder af en daarmee het risico op complicaties over de tijd steeds meer toe. Complicaties die in een gevorderd stadium van de ziekte mortaliteit kunnen veroorzaken zijn onder andere een aspiratiepneumonie of traumatisch letsel bij een val als gevolg van de houdingsinstabiliteit.
-
De diagnose wordt op basis van het klinisch beeld vastgesteld. Artsen gebruiken daarvoor de ‘MDS clinical diagnostic criteria for Parkinson’s Disease’. Er moet in ieder geval sprake zijn van bradykinesie in combinatie met een rusttremor of rigiditeit. Daarnaast kan de diagnose worden ondersteunt als er verbetering optreedt bij het geven van dopaminerge medicatie.
Bij onduidelijkheid over de diagnose kan er aanvullend onderzoek gedaan worden om andere oorzaken uit te sluiten of het dopaminetekort in de hersenen te bevestigen. Hierbij wordt gebruik gemaakt van MRI-scans of van nucleaire onderzoekstechnieken: SPECT (Single Photon Emission Computed Tomography) of PET (Positron Emission Tomography). In geval van uitgesproken cognitieve stoornissen kan een EEG (hersenfilmpje) bijdragend zijn [5]. Bij de PET- en SPECT-scan wordt gebruik gemaakt van een radioactieve stof die de zenuwuiteinden (terminals) van de dopaminerge neuronen zichtbaar maakt, om zo de mate van het verlies van nigrostriatale cellen (dopamine producerende cellen) vast te stellen.
-
De ziekte van Parkinson is niet te genezen. De behandeling is symptomatisch en bestaat primair uit het aanvullen van het tekort aan dopamine of het vervangen van dopamine. Daarvoor kunnen de volgende medicamenten worden voorgeschreven:
Levodopa. Deze stof is de voorloper van dopamine. Dopamine kan niet door de bloed-hersenbarrière en deze voorloper wel [6]. In de hersenen kan levodopa vervolgens door het lichaam worden omgezet in dopamine. Levodopa wordt altijd in combinatie met een zogenaamde decarboxylaseremmer, zoals carbidopa, gegeven. Dit is een stof die ook niet door de bloed-hersenbarrière kan komen en de omzetting van levodopa in dopamine buiten de hersenen remt. Hierdoor geeft levodopa weinig dopaminerge bijwerkingen in de periferie van het lichaam (zoals hypotensie en misselijkheid). Een ander middel wat gebruikt kan worden om te zorgen dat levodopa niet wordt afgebroken is een COMT-remmer (zoals entacapon). Het enzym catechol-O-methyltransferase (COMT) breekt levodopa namelijk af.
Dopamine-agonisten. Dit zijn stoffen die op dopamine lijken en via dopaminereceptoren de symptomen van de ziekte van Parkinson kunnen onderdrukken. Bij deze medicijnen treden vaker perifere dopaminerge bijwerkingen op, zoals misselijkheid en duizeligheid. Daarnaast leiden dopamine-agonisten vaker dan levodopa tot slaperigheid en impulscontrolestoornissen (zoals gok-, seks- of eetverslaving) [3]. Door het gebruik van dopamine-agonisten te staken of de dosering te verlagen, kan deze laatste stoornis worden verminderd of weer verdwijnen [6].
Daarnaast kunnen amantadine, MAO-B-remmers en anticholinergica worden voorgeschreven. De exacte werking van amantadine is niet bekend, maar men gaat ervan dat het de afgifte van dopamine stimuleert [7,8]. MAO-B-remmers zorgen ervoor dat het enzym monoamineoxidase-B wordt geremd. Hierdoor wordt er minder dopamine afgebroken. Anticholinergica kunnen helpen om de tremor te verminderen.
Tot slot kan een patiënt in aanmerking komen voor een hersenoperatie, een zogenaamde stereotaxie. Dit kan alleen als de klachten ernstig zijn en de motorische symptomen onvoldoende onderdrukt worden ondanks optimaal instellen op medicatie, of de behandeling met levodopa tot ernstige overtollige bewegingen, dyskinesieën, heeft geleid [5]. Daarbij wordt een gebied in de hersenen hoogfrequent gestimuleerd door Deep Brain Stimulation (DBS). Er wordt een elektrode diep in de hersenen geplaatst en een neurostimulator onder de huid aangebracht. Deze behandeling leidt tot een verbetering van de balans in de activiteit van de verschillende onderdelen van de basale ganglia en daarmee tot een vermindering van motorische symptomen. Ook DBS is een symptomatische behandeling die de progressie van de ziekte niet vermindert.
-
Auteurs
Auteur: Sarah Dekker, geneeskundestudent
Co-auteur: Lars Nijman, geneeskundestudent
Student reviewer: Emma Verdaasdonk, geneeskundestudent
Medisch specialist reviewer: H. Berendse, neuroloogLink voor verdieping
https://www.amboss.com/us/knowledge/Parkinson_disease/
Referenties
[1] Jameson, L. J., & Kasper, D. (2015). Harrison’s Principles of Internal Medicine (19th edition). McGraw-Hill Education.
[2] Ropper, A., & Samuels, M. (2019). Adams and Victor’s Principles of Neurology (11de editie). McGraw-Hill Education.
[3] Hersenstichting. (z.d.). Wat is de ziekte van Parkinson? Geraadpleegd op 8 januari 2022, van https://www.hersenstichting.nl/hersenaandoeningen/parkinson/
[4] Parkinson Vereniging. (z.d.). Impulscontrolestoornissen. Geraadpleegd op 8 januari 2022, van https://www.parkinson-vereniging.nl/archief/bericht/2021/01/28/Impulscontrolestoornissen
[5] Parkinson: over de ziekte | UMC Groningen. (z.d.). Geraadpleegd op 8 januari 2022, van https://www.umcg.nl/-/parkinson-over-de-ziekte
[6] Ziekte van Parkinson. (z.d.). NHG-Richtlijnen. Geraadpleegd op 8 januari 2022, van https://richtlijnen.nhg.org/standaarden/ziekte-van-parkinson#volledige-tekst
[7] Amantadine: drug information. (z.d.). Up To Date. Geraadpleegd op 28 maart 2022, van https://www.uptodate.com/contents/amantadine-drug-information
[8] Ritter, J., & Flower, R. J. (z.d.). Rang & Dale’s Pharmacology (8th edition). Elsevier Gezondheidszorg.
Kumar, V. (2013). Robbins Basic Pathology (9de editie). Elsevier.
Chou, K. L. (z.d.). Diagnosis and differential diagnosis of Parkinson’s disease. Up To Date. Geraadpleegd op 27 maart 2022, van https://www.uptodate.com/contents/diagnosis-and-differential-diagnosis-of-parkinson-disease
Pagina laatst bijgewerkt op 14-04-2022